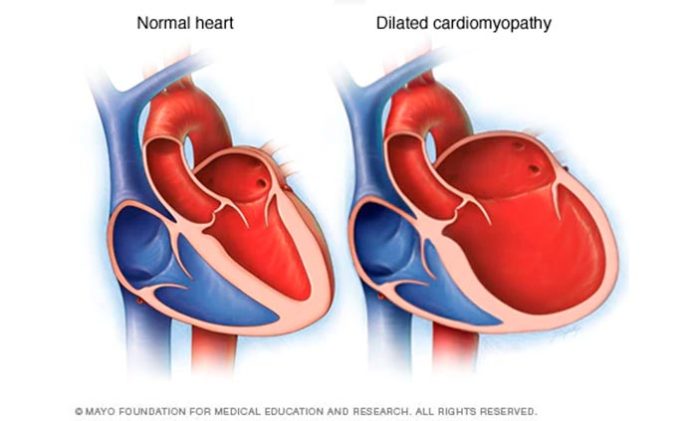
Científicos de la Escuela de Medicina Perelman de la Universidad de Pensilvania han descubierto las causas moleculares de una forma congénita de miocardiopatía dilatada (DCM), un trastorno cardíaco a menudo fatal.
Esta forma hereditaria de miocardiopatía dilatada, que a menudo causa muerte súbita o insuficiencia cardíaca progresiva, es uno de los múltiples trastornos congénitos que se sabe que son causados por mutaciones hereditarias en un gen llamado LMNA. El gen LMNA está activo en la mayoría de los tipos de células, y los investigadores no han entendido hasta ahora por qué las mutaciones de LMNA afectan órganos particulares como el corazón mientras que no afectan a la mayoría de los demás órganos y tejidos.
En el estudio, publicado esta semana en Cell Stem Cell, los científicos de Penn Medicine utilizaron técnicas de células madre para hacer crecer células del músculo cardíaco humano que contienen mutaciones que causan DCM en el gen LMNA. Descubrieron que estas mutaciones alteran gravemente la organización estructural del ADN en el núcleo de las células del músculo cardíaco, pero no otros dos tipos de células estudiadas, lo que conduce a la activación anormal de genes que no son del músculo cardíaco.
«Ahora estamos empezando a comprender por qué los pacientes con mutaciones en LMNA tienen trastornos de tejido restringido como la miocardiopatía dilatada, aunque el gen se expresa en la mayoría de los tipos de células«, afirma el coautor principal del estudio, Rajan Jain, doctor en Medicina y profesor asistente de Medicina Cardiovascular y Biología Celular y del Desarrollo en la Facultad de Medicina de Perelman.
Las mutaciones de LMNA que causan miocardiopatía dilatada habían comenzado a alterar la identidad de los cardiomiocitos, dándoles características de otros tipos de células
«El trabajo adicional en este sentido debería permitirnos predecir cómo se manifestarán las mutaciones de LMNA en pacientes individuales y, en última instancia, podríamos intervenir con fármacos para corregir la desorganización del genoma que causa estas mutaciones«, comenta el coautor principal del estudio, Kiran Musunuru, doctor en Medicina, profesor de Medicina Cardiovascular y Genética, y director del Programa de Orígenes Genéticos y Epigenéticos de Enfermedades en Penn Medicine.
Las mutaciones heredadas de LMNA han desconcertado a los investigadores durante mucho tiempo. El gen LMNA codifica proteínas que forman una estructura de encaje en la pared interna del núcleo celular, donde se alojan los cromosomas llenos de ADN enrollado. Esta estructura de encaje, conocida como lámina nuclear, toca algunas partes del genoma y estas interacciones lámina-genoma ayudan a regular la actividad genética, por ejemplo, en el proceso de división celular. El enigma es que la lámina nuclear se encuentra en la mayoría de los tipos de células, sin embargo, la alteración de este importante y casi ubicuo componente celular por mutaciones de LMNA provoca solo un puñado de trastornos clínicos relativamente específicos, incluida una forma de miocardiopatía dilatada, dos formas de distrofia muscular y una forma de progeria, un síndrome que se asemeja al envejecimiento rápido.
Para comprender mejor cómo las mutaciones de LMNA pueden causar DCM, Jain, Musunuru y sus compañeros de investigación tomaron células de un donante humano sano y utilizaron la técnica de edición de genes CRISPR para crear mutaciones conocidas de LMNA que causan miocardiopatía dilatada en cada célula. Luego utilizaron métodos de células madre para convertir estas células en células del músculo cardíaco (cardiomiocitos) y, a modo de comparación, en células hepáticas y grasas. Su objetivo era descubrir qué estaba sucediendo en los cardiomiocitos que contienen mutaciones que no sucedía en los otros tipos de células.
Los investigadores encontraron que en los cardiomiocitos mutantes en LMNA ─pero casi nada en los otros dos tipos de células─ la lámina nuclear tenía una apariencia alterada y no se conectaba con el genoma de la forma habitual. Esta alteración de las interacciones entre la lámina y el genoma provocó un fallo en la regulación genética normal: muchos genes que deberían desactivarse en las células del músculo cardíaco estaban activos. Los investigadores examinaron células tomadas de pacientes con miocardiopatía dilatada con mutaciones en LMNA y encontraron anomalías similares en la actividad genética.
Podrían abrirse nuevas vías de investigación que algún día podrían conducir al tratamiento o la prevención exitosos de las mutaciones de LMNA
Un patrón distintivo de actividad genética define esencialmente lo que los biólogos llaman la «identidad» de una célula. Así, las mutaciones de LMNA que causan DCM habían comenzado a alterar la identidad de los cardiomiocitos, dándoles características de otros tipos de células.
Los cardiomiocitos mutantes en LMNA también tenían otro defecto observado en pacientes con DCM ligada a LMNA: las células del músculo cardíaco habían perdido gran parte de la elasticidad mecánica que normalmente les permite contraerse y estirarse según sea necesario. No se observó la misma deficiencia en el hígado y las células grasas mutantes en LMNA.
Se están realizando investigaciones para comprender si los cambios en la elasticidad de las células del corazón con mutaciones de LMNA ocurren antes de los cambios en la organización del genoma, o si las interacciones del genoma en la lámina ayudan a garantizar la elasticidad adecuada. Sus experimentos sugirieron una explicación para las diferencias entre las conexiones entre la lámina y el genoma que están muy interrumpidas en los cardiomiocitos mutantes en LMNA, pero no tanto en las células adiposas y del hígado con mutaciones en LMNA: cada tipo de célula utiliza un patrón distinto de marcas químicas en su genoma, llamadas marcas epigenéticas, para programar sus patrones de actividad genética, y este patrón en los cardiomiocitos aparentemente da como resultado interacciones lámina-genoma que son especialmente vulnerables a la interrupción en presencia de ciertas mutaciones de LMNA.
«Los hallazgos revelan la probable importancia de la lámina nuclear en la regulación de la identidad celular y la organización física del genoma«, concluye Jain. «Esto también abre nuevas vías de investigación que algún día podrían conducir al tratamiento o la prevención exitosos de las mutaciones de LMNA y los trastornos relacionados«.
Fuente: Cell Stem Cell.