Investigadores de la Facultad de Medicina de la Universidad de Washington en St. Louis han identificado un proceso en las células inmunitarias que relaciona la deficiencia de vitamina D durante el embarazo con un mayor riesgo de diabetes tipo 2 en la descendencia. Los investigadores también encontraron que estas células inmunitarias y sus genes incorporados pueden usarse para transferir la diabetes tipo 2 a ratones sanos. La investigación se publica el hoy en Nature Communications, y el equipo tiene indicios de que este mecanismo también funcionaría en las personas.
Algunas teorías de la enfermedad sugieren que las condiciones en el útero pueden tener consecuencias irreversibles para toda la vida en la descendencia. El investigador principal del nuevo estudio, el doctor en medicina Carlos Bernal-Mizrachi, comenta que eso podría estar ocurriendo con los hijos de madres que no tienen niveles adecuados de vitamina D durante el embarazo.
«En estudios de ratones nacidos de madres con deficiencia de vitamina D, hemos encontrado que los animales desarrollan resistencia a la insulina y diabetes más adelante en la vida«
«La identificación de factores de riesgo ambientales modificables que pueden contribuir al desarrollo posterior de enfermedades metabólicas es fundamental para prevenir y tratar esas enfermedades«, asegura Bernal-Mizrachi, profesor de medicina en la División de Endocrinología, Metabolismo e Investigación sobre Lípidos. «Como la incidencia de diabetes y prediabetes se ha triplicado en las últimas décadas, particularmente en niños y adultos jóvenes, estamos analizando las condiciones ambientales durante el embarazo que pueden ayudar a explicar el aumento«.
Alrededor de 37 millones de estadounidenses han sido diagnosticados con diabetes y al menos 98 millones más tienen prediabetes, una condición caracterizada por la resistencia del cuerpo a la insulina. La deficiencia de vitamina D durante el embarazo puede ser uno de los factores que contribuyen a la resistencia a la insulina y al riesgo elevado de diabetes en la descendencia.
Los investigadores encontraron evidencia de que los mismos procesos que promueven la inflamación y la resistencia a la insulina en el tejido graso también funcionan en las personas
«En estudios de ratones nacidos de madres con deficiencia de vitamina D, hemos encontrado que los animales desarrollan resistencia a la insulina y diabetes más adelante en la vida«, recuerda Bernal-Mizrachi. «Eso fue cierto incluso cuando los cachorros fueron tratados con cantidades adecuadas de vitamina D después del nacimiento. Esos animales mejoraron su control de la glucosa, pero nunca se normalizaron«.
Los investigadores han identificado un tipo de célula madre que puede verse afectada de forma irreversible por la deficiencia de vitamina D durante el desarrollo en el útero. Las células madre se convierten en células inmunitarias y los investigadores descubrieron que podían trasplantar la diabetes a otros animales colocando estas células madre en ratones con niveles normales de vitamina D. Los investigadores concluyeron que los niveles insuficientes de vitamina D en el útero pueden programar las células inmunitarias para promover el desarrollo de la diabetes, proporcionando un objetivo para prevenir potencialmente este proceso.
Las dosis recomendadas no son suficientes
En esos experimentos, los investigadores encontraron que las células inmunitarias activaron un proceso genético que es el mismo proceso activado en las células inmunitarias recolectadas de madres que tenían niveles insuficientes de vitamina D cuando dieron a luz.
Aunque las vitaminas prenatales se recetan para asegurar niveles adecuados de nutrientes clave durante el embarazo, estos hallazgos de Bernal-Mizarachi y sus compañeros de investigación sugieren que las dosis recomendadas de vitamina D no son suficientes para normalizar los niveles de vitamina D en mujeres que tenían niveles bajos de vitamina D antes del embarazo.
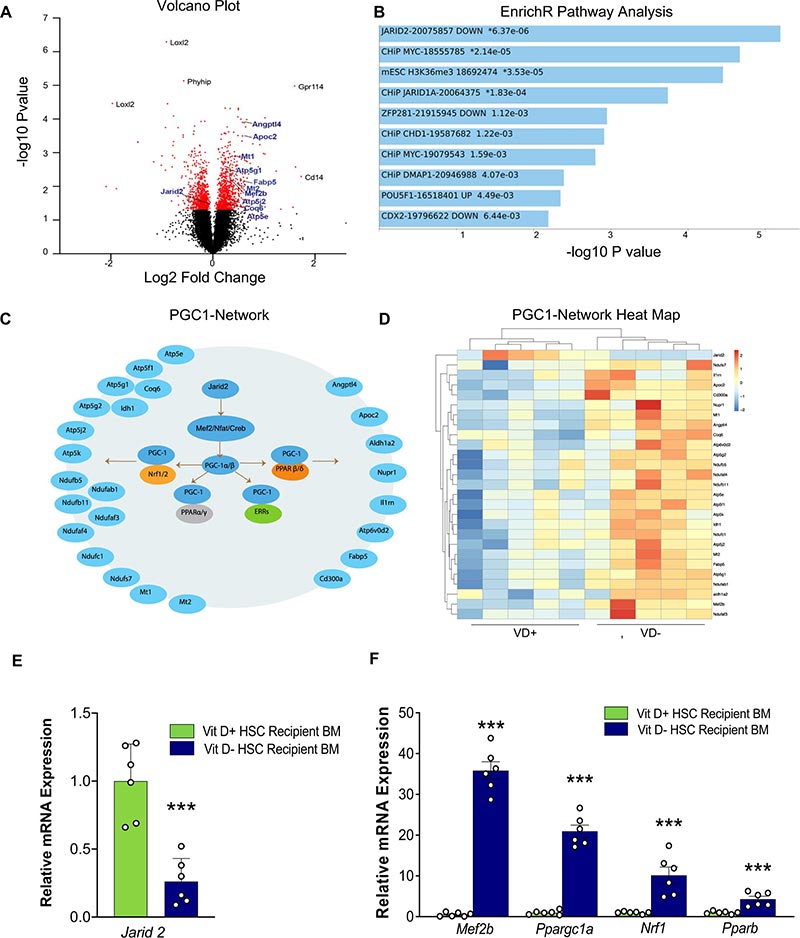
Alteraciones en genes específicos
El proceso que los investigadores identificaron en fetos de ratón se caracterizó por alteraciones en genes específicos. El programa genético modificado se identificó en las células madre que luego se convirtieron en células inmunitarias, incluidos los macrófagos. El equipo de investigación descubrió que estos macrófagos secretan una molécula que afecta la capacidad del tejido adiposo para almacenar glucosa, lo que aumenta los niveles de azúcar en la sangre.
«Los macrófagos que provienen de las células madre deficientes en vitamina D ingresan al tejido adiposo y contribuyen a la inflamación, lo que hace que el tejido adiposo se vuelva resistente a la insulina«, afirma Bernal-Mizrachi, quien también es jefe de medicina en Veterans Affairs St. Louis Health.
Es importante destacar que los investigadores encontraron evidencia de que los mismos procesos que promueven la inflamación y la resistencia a la insulina en el tejido graso también funcionan en las personas. Las células inmunitarias aisladas de la sangre del cordón umbilical de pacientes embarazadas con deficiencia de vitamina D que fueron atendidas por médicos de la Universidad de Washington mostraron cambios similares en los genes de las células inmunitarias y moléculas secretadas que se habían identificado previamente en ratones.
Fuente: Nature Communications.