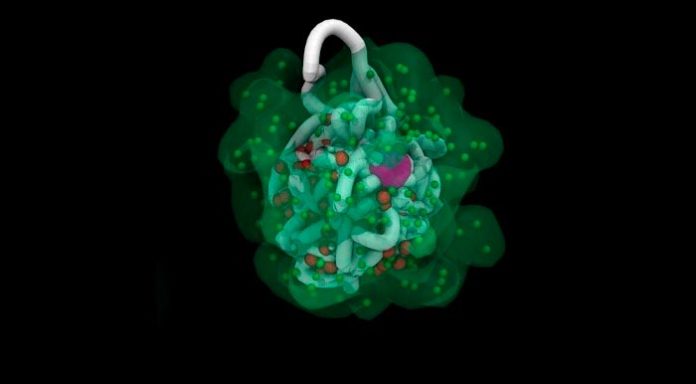

Usando modelos dinámicos impulsados por superordenadores basados en datos experimentales, los investigadores han podido observar el proceso que apaga un cromosoma X en embriones de mamíferos femeninos. Esta nueva capacidad está ayudando a los biólogos a comprender el papel del ARN y la estructura del cromosoma en el proceso de inactivación de X, lo que conduce a una comprensión más profunda de la expresión génica y abre nuevas vías para tratamientos farmacológicos para trastornos y enfermedades basados en genes.
«Esta es la primera vez que hemos podido modelar todo el ARN que se extiende alrededor del cromosoma y lo apaga«, asegura Anna Lappala, científica visitante en el Laboratorio Nacional de Los Alamos y física de polímeros en el Hospital General de Massachusetts y el Departamento de Harvard de Biología Molecular. Lappala es la primera autora del artículo publicado en Proceedings of the National Academy of Sciences (PNAS). «Sólo a partir de datos experimentales, que son 2D y estáticos, no tenemos la resolución para ver un cromosoma completo con este nivel de detalle. Con este modelo, podemos ver los procesos que regulan la expresión génica, y el modelo se basa en 2D datos experimentales de nuestros colaboradores en el Hospital General de Massachusetts y Harvard«.
«Nuestro principal objetivo era ver que el cromosoma X cambiaba de forma y ver los niveles de expresión génica a lo largo del tiempo»
El modelo, considerado 4D porque muestra movimiento, incluido el tiempo como cuarta dimensión, se ejecuta en superordenadores de Los Álamos. El modelo también incorpora datos experimentales de genomas de ratones obtenidos mediante un método molecular llamado 4DHiC. La metodología combinada molecular y computacional es de vanguardia.
En la visualización, las partículas de ARN pululan sobre el cromosoma X. Las hebras enredadas como espaguetis se retuercen, cambian de forma, luego las partículas se tragan y penetran en las profundidades del cromosoma, apagándolo.
«El método nos permite desarrollar un modelo interactivo de este proceso epigenético«, afirma Jeannie T. Lee, profesora de Genética en la Escuela de Medicina de Harvard y vicepresidenta de biología molecular en el Hospital General de Massachusetts, cuyo laboratorio contribuyó con los datos experimentales que sustentan el modelo.
La epigenética es el estudio de los cambios en la expresión génica y los rasgos hereditarios que no implican mutaciones en el genoma.
«Lo que faltaba en este campo es alguna forma de que un usuario que no tiene conocimientos de computación acceda de forma interactiva a un cromosoma«, comenta Lee. Ella comparó el uso del modelo de Los Álamos con el de Google Earth, con el que «puedes hacer zoom en cualquier lugar de un cromosoma X, elegir tu gen favorito, ver los otros genes que lo rodean y cómo interactúan«. Esa capacidad podría dar una idea de cómo se propagan las enfermedades, por ejemplo, según Lee.
Modelo 4D
Basado en el trabajo en este documento, Los Álamos está desarrollando actualmente un navegador estilo Google Earth donde cualquier científico puede cargar sus datos genómicos y verlos dinámicamente en 3D con varios aumentos, indica Karissa Sanbonmatsu, bióloga estructural del Laboratorio Nacional de Los Álamos, autora del artículo y líder del proyecto en el desarrollo del método computacional.
En los mamíferos, un embrión femenino se concibe con dos cromosomas X, uno heredado de cada padre. La inactivación de X apaga el cromosoma, un paso crucial para que el embrión sobreviva, y las variaciones en la inactivación de X pueden desencadenar una variedad de trastornos del desarrollo.
El nuevo modelo de Los Álamos facilitará una comprensión más profunda de la expresión génica y los problemas relacionados, lo que podría conducir a tratamientos farmacológicos para diversas enfermedades y trastornos genéticos, según Lee. «Nuestro principal objetivo era ver que el cromosoma cambiaba de forma y ver los niveles de expresión génica a lo largo del tiempo«, agrega Sanbonmatsu.
«La hipótesis es que un cromosoma compactado y estructurado de manera estrecha tiende a desactivar los genes»
Para comprender cómo se activan y desactivan los genes, sigue Sanbonmatsu, «realmente es útil conocer la estructura del cromosoma X. La hipótesis es que un cromosoma compactado y estructurado de manera estrecha tiende a desactivar los genes, pero no hay muchas pistas sobre esto. Al modelar estructuras 3D en movimiento, podemos acercarnos a la relación entre la compactación estructural y la desactivación de genes«.
Lee comparó la estructura del cromosoma con el origami. Una forma complicada similar a una grulla de origami ofrece mucha superficie para la expresión genética y podría ser biológicamente preferida para permanecer activa.
El modelo muestra una variedad de subestructuras en el cromosoma. Cuando se cierra, «es un proceso fragmentado en el que se mantienen algunas subestructuras pero otras se disuelven«, afirma Sanbonmatsu. «Vemos las etapas inicial, intermedia y final a través de una transición gradual. Eso es importante para la epigenética porque es la primera vez que hemos podido analizar la transición estructural detallada en un cambio epigenético«.
Una X inactiva puede activarse más tarde en un proceso llamado activación de X inactiva relacionada con la edad
El modelo también muestra genes en la superficie del cromosoma que escapan a la inactivación del cromosoma X, lo que confirma los primeros trabajos experimentales. En el modelo, se agrupan y aparentemente interactúan o trabajan juntos en la superficie del cromosoma.
En otra perspectiva del modelo, «A medida que el cromosoma pasa de un X activo, cuando todavía es bastante grande, a un X compacto inactivo, que es más pequeño, notamos que hay un núcleo del cromosoma que es extremadamente grande y denso, pero la superficie es mucho menos densa. También vemos mucho más movimiento en la superficie«, indica Lappala. «Luego, hay una región intermedia que no es demasiado rápida o lenta, donde el cromosoma puede reorganizarse«.
Una X inactiva puede activarse más tarde en un proceso llamado activación de X inactiva relacionada con la edad. «Se asocia con problemas en las células sanguíneas en particular que se sabe que causan autoinmunidad«, asegura Lee. «Algunas investigaciones intentan farmacológicamente activar el X inactivo para tratar trastornos neurológicos en los niños devolviéndoles algo que falta en su cromosoma X activo. Por ejemplo, un niño podría tener una mutación que puede causar una enfermedad. Pensamos que, si podemos reactivar la copia normal en la X inactiva, entonces tendríamos un tratamiento epigenético para esa mutación«.
Fuente: bioRxiv.




















